2025年5月4~7日,第93届欧洲动脉粥样硬化学会年会(EAS 2025)在英国格拉斯哥隆重召开。作为动脉粥样硬化领域的国际交流平台,EAS大会精英荟萃,分享最新研究成果和临床经验。其中,血脂管理作为动脉粥样硬化性心血管疾病(ASCVD)的重要防治手段之一,尤以低密度脂蛋白胆固醇(LDL-C)为主要靶标,亦为会议焦点及学术热点。本文全面整理相关数据,带您速览血脂前沿进展,涵盖从管理理念、治疗路径到创新药物如小干扰RNA(siRNA)降胆固醇药等最新数据。
一、ASCVD防治新理念:从心血管事件链看LDL-C管理之重要性
目前,“心血管事件链”概念已成为ASCVD管理和防治的重要理论基础。在心血管事件链视角下,ASCVD发生发展是一个持续进展的过程,涵盖从心血管危险因素、靶器官损害到心血管疾病的各个阶段。基于心血管事件链,ASCVD防治新理念强调早期、全程及综合管理,其中血脂管理必不可少。鉴于LDL-C与心血管风险之间具有明确的因果关系,LDL-C已成为公认的血脂管理主要靶标。
EAS会议再次强调在ASCVD发展全程中对极高危患者LDL-C管理的重要性。德国莱比锡大学研究者通过分享4个病例,包括纯合子家族性高胆固醇血症伴黄瘤儿童患者,以及急性冠脉综合征(ACS)、ACS后Wellens综合征、慢性冠脉综合征(CCS)等成年患者,详细阐述ASCVD全程强效降低LDL-C水平对于改善动脉粥样硬化、稳定斑块的重要性(图1)[1,2]。
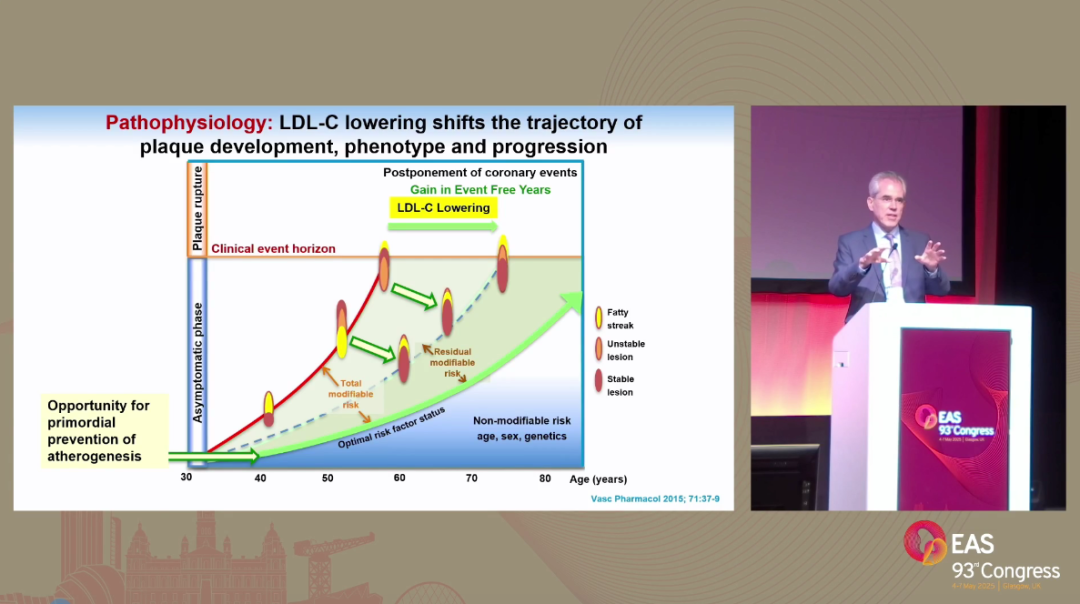
图1. LDL-C降低改变ASCVD发展轨迹[2]
二、LDL-C管理路径:早期、强化干预,探索联合治疗达标路径
早期干预及强化干预的重要性
除LDL-C水平外,LDL-C累积暴露也与ASCVD风险显著相关。因此,国内外血脂指南一致推荐早期及强化干预为LDL-C管理重要策略,LDL-C降低不仅强调“更低更好”(Lower is better),也要“更长更稳”(Lower for longer)。对于已确诊ASCVD患者,2019 ESC/EAS血脂管理指南建议降脂目标为LDL-C<1.4 mmol/L且较基线降低幅度≥50%[3];2023中国血脂管理指南建议极高危患者LDL-C目标值为<1.8 mmol/L且较基线降幅>50%,超高危患者<1.4 mmol/L且较基线降幅>50%[4]。
本次EAS会议在“强化与早期LDL-C治疗的适用人群”专场中,讨论了如何识别心血管极高危患者。对于既往无心血管疾病人群,推荐使用欧洲系统性冠状动脉风险评估2(SCORE2)和SCORE2-老年人(SCORE2-OP)评分进行风险分层,以预测10年内发生心血管疾病的风险。确诊ASCVD患者、糖尿病伴靶器官损害、重度肾功能不全等患者可直接判定为心血管极高危人群[3]。识别出极高危患者后,应及时干预以使LDL-C尽快达标。
LDL-C联合治疗达标路径探索
对于极高危/超高危ASCVD患者,为尽快实现并长期维持LDL-C达标,通常需要联合应用降脂药物。传统上的降脂联合治疗一般采取阶梯疗法,然而目前越来越多证据支持早期联合策略,EAS会议对优化LDL-C联合治疗的达标路径进行了探索。
德国亚琛大学医院研究者展示了早期联合以获得降低LDL-C最佳水平的新证据。在瑞典SWEDEHEART大规模注册研究(n=35,826)中,比较了心肌梗死术后患者在他汀基础上早期联合(出院后12周内联合)与晚期联合(出院后13周~16个月联合)的不同结局。结果显示,与晚期联合相比,早期联合患者的LDL-C达标率更高(38.4% vs. 28.8%,图2),主要心血管不良事件(MACE)和心血管死亡风险显著降低,其中3年MACE风险下降14%。据模型推测,在SWEDEHEART样本量人群中,若所有患者均早期联合,可减少477例MACE事件(图3)[5]。该研究结果强力支持,早期联合通过改善LDL-C达标率来改善临床不良结局,从而挽救更多生命。
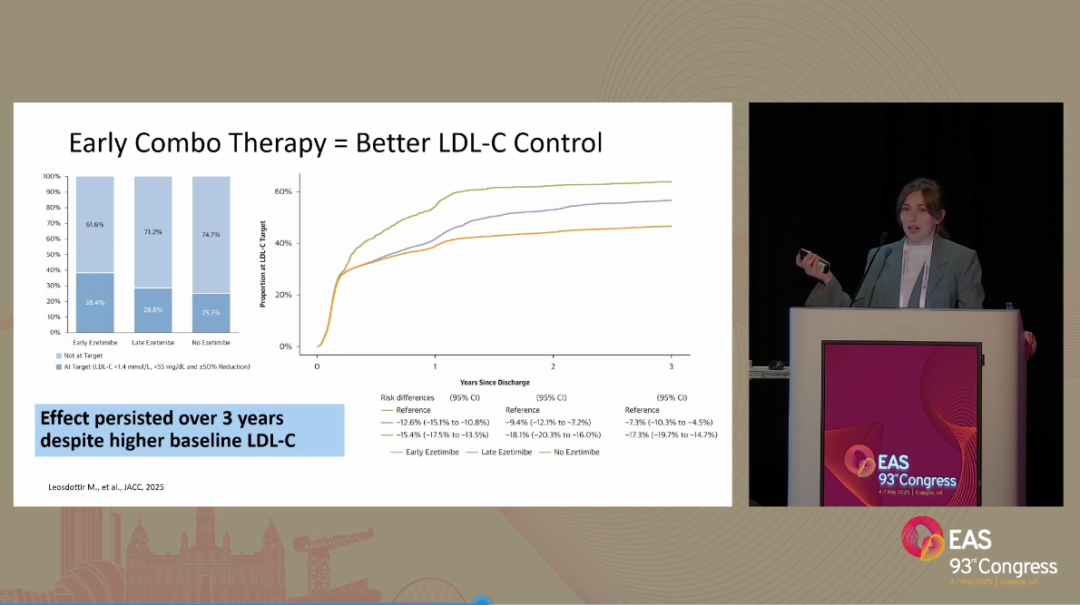
图2. 早期联合降脂提高LDL-C达标率

图3. 早期联合降脂治疗降低心血管风险
近年来,关于联合降脂疗法的呼声越来越高,2025年3月《欧洲心脏杂志:心血管药物治疗》在线发表了《关于将联合疗法整合到血脂异常管理治疗方案的专家意见》[6],EAS会议对此进行专门介绍和探讨。最新专家建议:治疗模式应从高强度他汀转变为高强度降脂治疗,并优先考虑一线联合降脂治疗,以克服不充分血脂管理带来的残余心血管风险[6]。此观点与刚刚结束的ACC大会公布指南不谋而合。2025 ACC ACS指南新增推荐,无论对于最大耐受剂量他汀治疗且LDL-C不达标的ACS患者,还是他汀类不耐受的ACS患者,应用非他汀类药物(包括英克司兰)治疗;对于英克司兰等PCSK9靶点类药物,无需等到依折麦布治疗不达标再加用,提升了推荐等级,有助于LDL-C早期达标[7]。
三、创新降脂药物进展:英克司兰一年两针*,助力实现LDL-C长期达标
从医患视角看降脂治疗障碍:依从性是重要因素
从循证到指南均强力支持LDL-C达标的重要性,但临床实践中血脂管理现状欠佳。临床上阻碍降脂治疗的障碍有很多,其中依从性问题不容忽视。EAS会议上报道的一项土耳其调查研究显示从医生角度,患者依从性(38.71%)、医患合作(22.59%)、患者教育(18.94%)是实现LDL-C达标率最主要的三大障碍,其中依从性问题居首位[8];从患者角度,中断降脂治疗的主要原因包括无症状、用药太多和担心副作用等,其中因服药太多而停止降脂治疗的患者占比高达38.26%~46.48%[9]。因此,临床亟需能够提高治疗依从性的创新疗法,依从性对于实现长期达标起着关键作用,具有依从性优势的药物也因此成为领域关注热点。
真实世界研究新证:英克司兰助力ASCVD患者实现长期LDL-C达标
多项临床研究已证实,英克司兰可维持6个月的超长药效,一年两针*即可助力ASCVD患者LDL-C更低更持久地达标[10-16]。VICTORION-INITIATE研究显示,ASCVD患者采用“英克司兰优先”策略(最大耐受他汀治疗未实现LDL-C<1.8 mmol/L时立即加用英克司兰),相较常规治疗能更快且持续实现LDL-C达标[17]。同时,英克司兰全球真实世界证据也在不断积累,本次EAS会议上报道了多项新研究。
比利时注册研究(BE.REAL)是一项非干预性真实世界研究,揭示英克司兰在ASCVD患者中降低LDL-C的疗效[18]。本次中期分析共纳入297例应用英克司兰的ASCVD患者,近半数患者接受4针治疗,基线LDL-C水平为137.4 mg/dL。评估英克司兰每次注射期间(0~3个月、3~9个月和9~15个月)的LDL-C降低效果。结果显示,英克司兰使患者在最长15个月内持续显著降低LDL-C水平达42.6%~47.3%,且坚持他汀+依折麦布为背景治疗的患者LDL-C持续降幅最大,在起始3个月降幅即达57.3%,且在后续治疗期间维持降幅在52.6%~54.6%(图4)[18]。

图4. 英克司兰治疗降低LDL-C的相对(a)和绝对(b)降幅
在一项小规模印度前瞻性真实世界研究中,纳入31例既往伴或不伴ASCVD病史的患者,评估英克司兰的降脂疗效。结果显示,起始英克司兰治疗3个月后,96.15%患者实现LDL-C降幅>50%,84.62%患者实现LDL-C<1.4 mmol/L[19]。另一项EAS公布的研究纳入30例既往降脂治疗不达标联合应用英克司兰的CCS患者,随访1年LDL-C降幅达61%(P<0.001),达标率90%(LDL-C<70 mg/dL),值得注意的是同时hs-CRP降低25%(P<0.05),这为英克司兰抗炎作用提供了线索[20]。
以上新证据与既往全球发表的众多真实世界研究结果相似,一致支持英克司兰在临床实践中可有效降低ASCVD患者LDL-C水平,助力更多患者实现长期LDL-C达标。
总结
EAS2025会议全面展现了血脂前沿最新进展。以LDL-C为主要标靶的血脂管理对于ASCVD全程防治至关重要,新理念强调早期、强化降脂干预,并积极探索优化联合治疗路径。值得注意的是,目前血脂管理仍面临达标率低、依从性欠佳等挑战,siRNA药物英克司兰为降脂治疗不达标患者提供突破性解决方案,其强效降脂作用在此次EAS会议公布的研究中再次得以证实。
此外,除传统LDL-C靶点外,非LDL-C靶点如脂蛋白(a)、甘油三酯、载脂蛋白C-III(APOC-III)等也受到越来越多的关注。相信随着创新疗法不断取得进展,血脂管理也将朝着更高效、更便利、更安全的方向不断迈进。
* 首针后三个月注射加强针,此后仅需一年两针维持治疗
参考文献:
1. Ulrich Laufs. Very high cardiovascular patients risk profiles across the ASCVD continuum. Presented at EAS2025.
2. Packard CJ, et al. Vasc Pharmacol. 2015; 71: 37-39.
3. Mach F, et al. Eur Heart J. 2020; 41(1): 111-188
4. 中国血脂管理指南修订联合专家委员会. 中国血脂管理指南(2023年). 中华心血管病杂志. 2023; 51(3): 221-255.
5. Leosdottir M, et al. J Am Coll Cardiol. 2025; 85(15): 1550-1564.
6. Parhofer KG, et al. Eur Heart J Cardiovasc Pharmacother. 2025 Mar 6: pvaf007.
7. Rao SV, et al. Circulation. 2025; 151(13): e771-e862.
8. Ozdogan O, et al. Barriers to lipid lowering therapy in Turkiye: Physician’s perspective (B-Aware dyslipidemia). Presented at EAS2025. 139.
9. Ozdogan O, et al. Barriers to lipid lowering therapy in Turkiye: Patient’s perspective (B-Aware dyslipidemia). Presented at EAS2025. 138.
10. Khvorova A. N Engl J Med. 2017; 376(1): 4-7.
11. Lancellotti P, et al. N Engl J Med. 2017; 376(18): e38.
12. Do RQ, et al. Curr Cardiol Rep. 2013; 15(3): 345.
13. Weng Y, et al. Biotechnol Adv. 2019; 37(5): 801-825.
14. Brown, C. R., Evidence for an Intracellular Depot that Contributes to the Extended Duration of Activity of GalNAc-siRNA Conjugates. 2020.
15. Dyrbu? K, et al. J Clin Lipidol. 2020; 14(1): 16-27
16. Fitzgerald K, et al. N Engl J Med. 2017; 376(1): 41-51.
17. Koren MJ, et al. J Am Coll Cardiol. 2024; 7: S0735-1097(24)06624-5.
18. Fabian Demeure, et al. Real-world adherence, LDL-C lowering effect and goal-attainment of inclisiran in Belgian patients with atherosclerotic cardiovascular disease: The BE.REAL registry. Presented at EAS2025.
19. Yalamanchi RP, et al. ACHIEVING LDL-C GOALS WITH INCLISIRAN: INSIGHTS FROM AN INDIAN PROSPECTIVE STUDY. Presented at EAS2025.
20. Rano B. Alieva, et al. THE IMPACT OF ONE-YEAR INCLISIRAN TREATMENT ON ACHIEVING TARGET LOW-DENSITY LPOPROTEIN CHOLESTEROL LEVELS IN PATIENTS WITH CHRONIC CORONARY SYNDROME. Presented at EAS2025.
审批码LEQ0045639-98195,有效期为2025-05-06至2026-05-05,资料过期,视同作废
我要留言